推荐产品
技术资料/正文
赛多利斯制药 QC合规解决方案(符合《2025版中国药典》要求)
255 人阅读发布时间:2025-08-28 11:25
满足《2025版中国药典》(包括“9032分析用电子天平称量指导原则”、“9209制药用水微生物监测和控制指导原则”、“通则1101 无菌检查法”)要求的制药 QC 解决方案。
赛多利斯提供创新的制药质量控制(QC)仪器和耗材,旨在赋能制药企业高效合规地简化流程,确保结果准确可靠,并维持产品安全性和效价的高标准。
新版《2025中国药典》制药 QC相关指导原则解读
<9032分析用电子天平称量指导原则>
2025版《中国药典》新增<9032分析用电子天平称量指导原则>,从概念定义到性能核查,再到规范管理和实操要求,无一不体现着更严谨、更精细的质量控制理念。这不仅是对实验室称量操作的更高要求,更是对数据完整性与结果可靠性的再次强调。
-
明确概念:明确了天平的适用范围与使用场景;细化了仪器确证(IQ/OQ/PQ)的流程与要求;强调了校准与校正的周期性、准确性及溯源性。
-
性能核查:更加强调对天平准确度、重复性等关键性能的核查,并引入了最小准确称量值(Mmin)和最小样品量(Msnw)等概念,旨在确保每次称量结果的有效性与可信度。
-
规范管理:对环境要求、安装要求、日常使用与维护提出了更严格的规范,强调环境对称量结果的影响。
-
强调实操:针对称量容器、称量操作方法以及特殊样品处理与安全性等方面提出了具体要求。
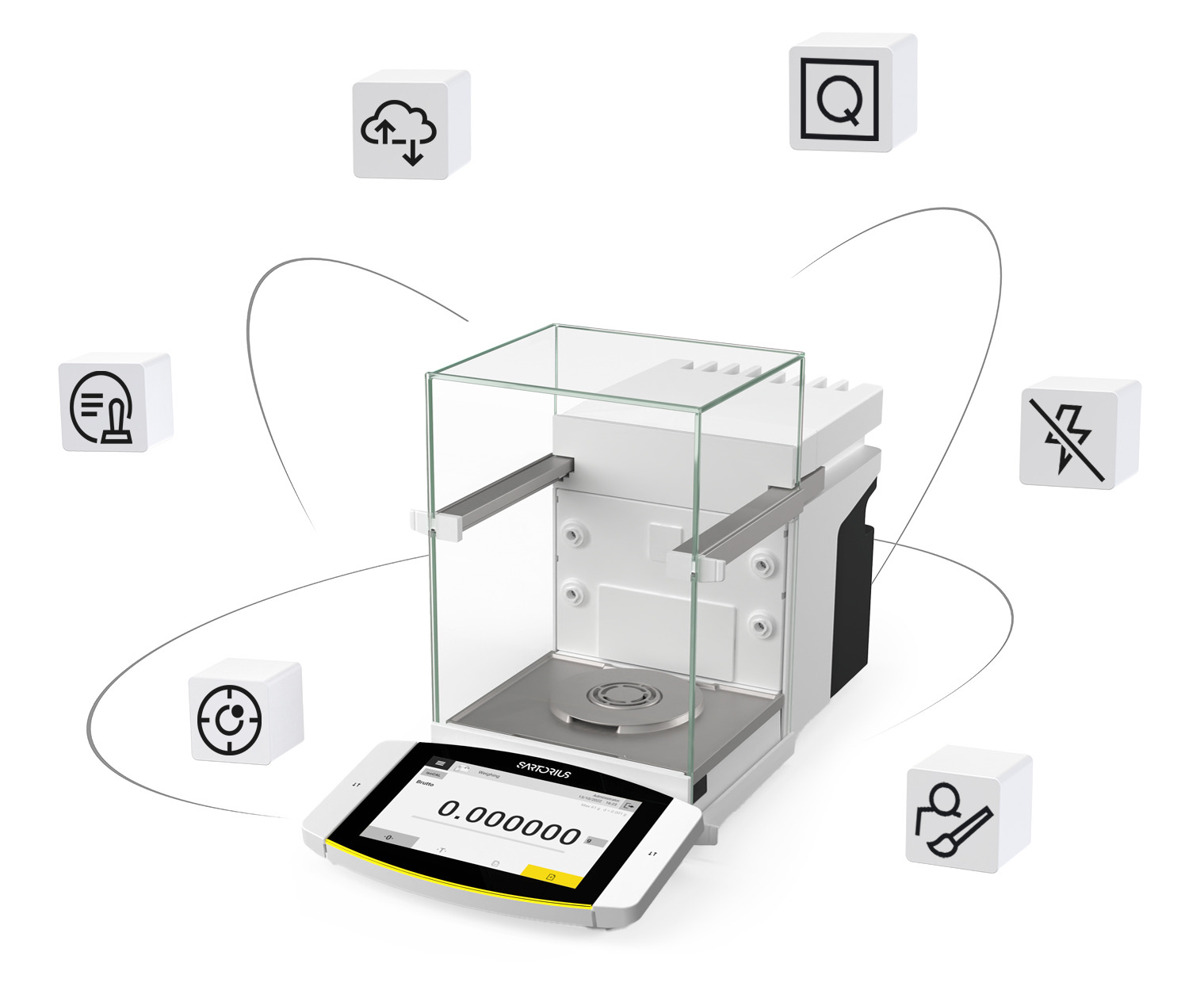
赛多利斯的高性能的天平,提供全面、智能、符合未来趋势的药典合规解决方案:
-
超级单体传感器,力求理想最小准确称量值
-
静电消除零死角,轻松“稳”住称重结果
-
容器选择无限制,保持稳定的重复性偏差
<9209制药用水微生物监测和控制指导原则>
新增<9209制药用水微生物监测和控制指导原则>包括了制药用水中微生物的特点、微生物监测、微生物控制与风险提示等,新规不仅强调了微生物监测的全面性要求与控制的有效性措施,更要求将风险管理理念贯穿于制药用水系统的整个生命周期。
-
原水控制:强调制定原水可接受标准(微生物、细菌内毒素),并实施预处理措施,关注环境季节影响。
-
系统设计:关注系统工艺选择、设备材质、防污染设计及消毒措施,避免微生物滋生。
-
系统确认:细化确认阶段取样、微生物检测方法验证及清洁消毒程序验证。
-
持续监控:要求持续监控水质,定期风险评估,并对异常结果进行根本原因分析与纠正。
-
其他措施与风险提示:强调防污染设计、定期消毒/滤材更换,并关注寡营养型微生物的监测。
赛多利斯Arium系列纯水系统,符合药典实验室用水要求:
1. 全面的微生物风险管理
-
独特的生物级袋式水箱,从源头抑制生物膜
-
优化流路设计及多重屏障,实现全流程微生物防控
-
智能监控-电导率与TOC监测,完全符合2025版中国药典要求
2. 全方位合规支持
-
标准化IQ/OQ文件与现场服务,助力系统全程符合GMP法规
-
灵活维护方案,保障系统长期稳定可靠运行

<通则1101 无菌检查法>
2025版《中国药典》对<通则1101 无菌检查法>进行了修订与优化,旨在降低假阳性(环境/操作污染)和假阴性(抑菌性)风险,确保无菌检测结果的准确性。
-
无菌环境与操作:强调无菌检查需在严格无菌条件下进行,全过程须遵守无菌操作,环境监测与控制的重要性不变,但删除了对特定国标(GB1629系列)的强制引用。
-
培养基适用性检查:要求“每批”培养基(含自制与商品化)均需进行无菌性和灵敏度适用性检查。
-
供试品和抑菌性:降低冲洗量,一般不得超过5次,每次100ml;强调即使方法适用性验证无法完全消除抑菌性,最大冲洗量亦不得增加。
-
生物制品检测:取消生物制品无菌检测额外制备一份FTM培养基的规定;生物制品不再享有特殊分类和检测要求,实现与各类药品检测规则统一。
赛多利斯 Sterisart® 全封闭无菌检查系统,为您提供从样品处理到结果判读的全流程、高合规性的无菌检测解决方案,帮助您轻松应对新规挑战。
-
Sterisart® Universal第四代无菌检测泵结合Sterisart® 无菌滤筒,全封闭系统防止环境与操作污染
-
高效消除抑菌性,适配药典低冲洗量要求,确保检测结果的真实准确性(真阳/真阴),加速产品放行
-
智能简化操作: 即用型耗材与高度标准化流程,降低人为误差,提升实验室操作安全性与整体效率,轻松应对药典多变需求

针对不同种类药物,赛多利斯提供个性化解决方案。
| 生物药解决方案 | 化药解决方案 | 中药解决方案 |
| 针对生物药复杂挑战,赛多利斯提供靶点亲和力、AAV滴度、细胞活力等前沿分析方案;同时,以符合药典趋势的快速无菌检测替代方法,加速产品放行,推动生物药研发与生产效率。 | 先进的无菌样品检测方案(符合ChP 1101)能降低假阳性,确保安全放行;高品质超纯水(符合药典9209)以及高效杂质分析样品预处理工具,提升色谱分析精度,保障产品纯度与安全。 | 赛多利斯中药方案,确保中药标准品称量的精准度与数据完整性(符合药典9032),并提供超纯水(符合药典9209)保障重金属/痕量分析的纯净与准确性,助力中药现代化标准提升。 |
更多符合《2025版中国药典》的制药QC合规解决方案,欢迎联系赛多利斯!







